癌症免疫疗法已成为肿瘤学的一种变革性方法,其中免疫检查点抑制剂 (ICI) 处于最前沿。ICI通过阻断T细胞中的调节途径起作用,癌细胞利用这些途径逃避免疫检测。
免疫检查点抑制剂的机制
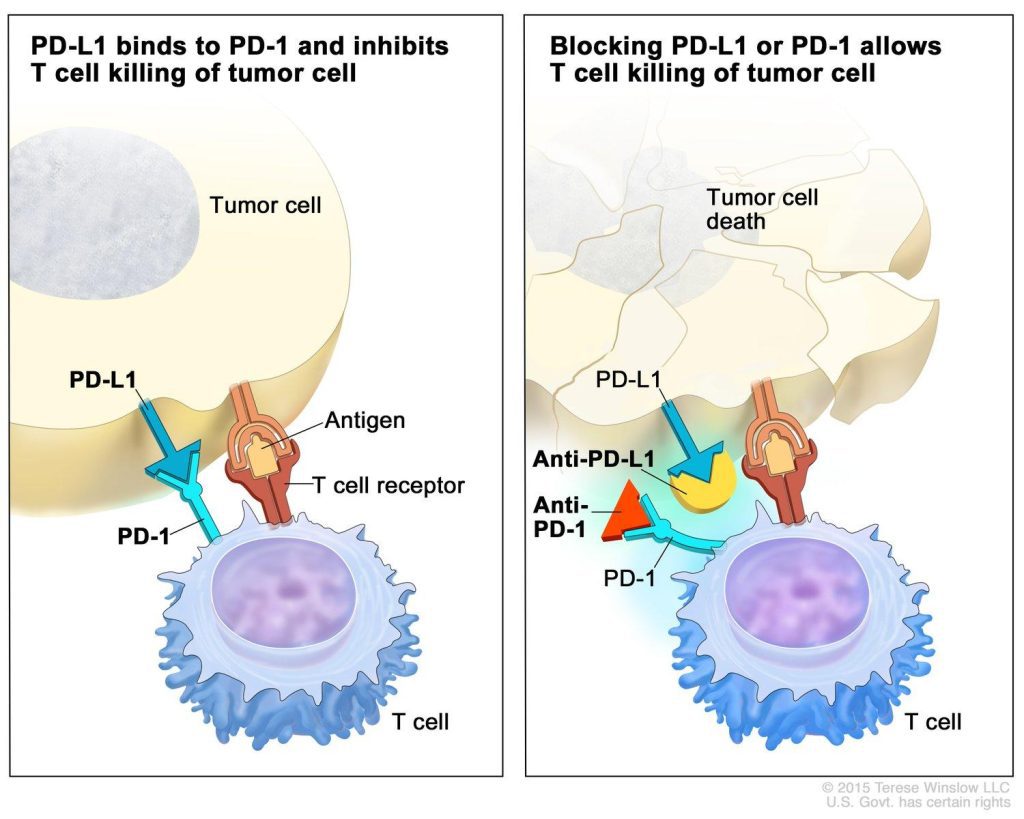
免疫检查点是维持自我耐受并调节生理性免疫反应的持续时间和幅度的调节途径。研究最充分的检查点是细胞毒性 T 淋巴细胞相关蛋白 4 (CTLA-4) 和程序性死亡 1 (PD-1) 及其配体 PD-L1。肿瘤细胞经常利用这些途径来避免免疫监视。
CTLA-4 在 T 细胞上表达,并作为 T 细胞活化的负调节因子。Ipilimumab 是一种针对 CTLA-4 的单克隆抗体,是 FDA 批准的第一个用于治疗转移性黑色素瘤的 ICI。通过阻断CTLA-4,ipilimumab增强T细胞活化和增殖,从而增强抗肿瘤免疫力。
PD-1在T细胞表面表达,其与在肿瘤细胞上表达的PD-L1相互作用,导致T细胞活性的抑制。单克隆抗体(如帕博利珠单抗和纳武利尤单抗)靶向 PD-1,而阿替利珠单抗靶向 PD-L1,可防止这种相互作用并恢复 T 细胞功能。
免疫检查点抑制剂的临床应用
ICI 已在多种恶性肿瘤中显示出显着的疗效,包括黑色素瘤、非小细胞肺癌 (NSCLC)、肾细胞癌 (RCC) 和霍奇金淋巴瘤。ICIs的临床成功导致其迅速被采用并整合到标准的癌症治疗方案中。
在黑色素瘤中使用 ipilimumab 是癌症治疗的关键时刻,表明晚期疾病患者的总生存期有所改善。随后对 PD-1 抑制剂的研究进一步延长了生存获益,将 ICI 确立为黑色素瘤的标准治疗。
ICIs在非小细胞肺癌(NSCLC)中显示出显著的疗效,特别是在PD-L1高表达的患者中。帕博利珠单抗联合化疗已成为转移性非小细胞肺癌的一线治疗药物,其生存结局显著改善。
在肾细胞癌 (RCC) 中,与依维莫司相比,纳武利尤单抗在既往接受过治疗的患者中显示出更高的总生存期。纳武利尤单抗和伊匹木单抗的联合治疗也已获批用于一线治疗,凸显了ICI联合治疗的潜力。
ICI与抗体疗法之间的协同作用
抗体-药物偶联物 (ADC) 将单克隆抗体的特异性与化疗的细胞毒性潜力相结合,提供靶向递送治疗药物。将ADC与ICI结合,不仅可以直接杀死肿瘤细胞,还可以增强免疫识别和反应,从而增强抗肿瘤免疫力。
双特异性抗体被设计为同时结合两种不同的抗原,从而可以将免疫细胞重定向到肿瘤细胞。双特异性抗体与ICI的结合可以增强肿瘤部位T细胞的募集和活化,为癌症治疗提供多方面的方法。
挑战与未来方向
ICI的主要挑战之一是免疫相关不良事件(irAEs)的管理,这些不良事件可以影响任何器官系统,并且严重程度各不相同。了解 irAE 的潜在机制并制定缓解它们的策略对于更广泛地应用 ICI 至关重要。
识别预测对 ICI 反应的生物标志物对于优化患者选择和治疗结果至关重要。PD-L1 表达、肿瘤突变负荷 (TMB) 和微卫星不稳定性 (MSI) 目前正在作为潜在的生物标志物进行研究。
ICI的未来在于它们与其他治疗方式的整合,包括靶向治疗、放疗和其他免疫治疗。临床前和临床研究正在进行中,以确定最有效的组合和治疗顺序。
免疫检查点抑制剂代表了癌症治疗的重大进步,为以前无法治疗的恶性肿瘤患者提供了新的希望。它们与抗体疗法的整合呈现出一个有前途的前沿,结合了两种方法的优势来增强抗肿瘤功效。正在进行的研究和临床试验将继续完善这些疗法,旨在最大限度地发挥其益处,同时最大限度地减少不良反应。
参考资料:
- Shiravand,Y.,Khodadadi,F.,Amin Kashani,SM,Hosseini-Fard,SR,Hosseini,S.,Sadeghirad,H.,Ladwa,R.和Kulasinghe,A.(2022)。癌症治疗中的免疫检查点抑制剂。当代肿瘤学,29(5),3044-3060。https://doi.org/10.3390/curroncol29050247