弗吉尼亚大学研究人员的一篇综述强调了抗体依赖性细胞吞噬作用 (ADCP) 在癌症免疫疗法中的作用。非偶联单克隆抗体 (mAb) 通过靶向恶性细胞上的特异性抗原对癌症治疗产生了重大影响。广泛使用的单克隆抗体,如抗CD20(利妥昔单抗、奥妥珠单抗)、抗HER2(曲妥珠单抗)和抗CD38(达雷妥尤单抗),使用ADCP靶向和去除恶性细胞。然而,作为单一疗法,这些单克隆抗体在体内通常产生的细胞毒性不足,并且在联合疗法中更有效。此外,耐药性的发展也是一个重大挑战。
FcγR 介导的 ADCP
Fcγ受体(FcγRs)对ADCP至关重要。这些受体存在于巨噬细胞等免疫细胞上,与IgG抗体的Fc部分结合。FcγR分为激活受体和抑制受体,它们的激活由这些受体在细胞表面的结合比例决定。不同 IgG 亚类的结合特异性和亲和力增加了该系统的复杂性。高亲和力受体通常被单体 IgG 饱和,而低亲和力受体在免疫反应期间结合免疫复合物。
FcγR 介导的吞噬作用的激活涉及三个步骤:配体-受体结合、受体聚集和磷酸化以及肌动蛋白驱动的吞噬。该过程导致吞噬体的形成,吞噬体通过与内体和溶酶体融合而成熟,导致靶细胞降解。吞噬体的酸化增强了其降解能力,这一过程受 NADPH 氧化酶和其他酶的调节。
补体 ADCP
补体系统是一种古老的免疫监视系统,通过用补体片段(如 C3b 和 iC3b)调理靶细胞在 ADCP 中发挥作用。免疫细胞上的补体受体 (CR) 识别这些片段,促进吞噬作用。由于 CR3 对 iC3b 的高亲和力,它被认为是补体介导的吞噬作用的关键介质。补体激活涉及三种途径——经典途径、凝集素途径和替代途径——所有途径都在 C3 转化酶的形成时汇聚。
补体和FcγR ADCP之间的协同作用
FcγRs 和 CRs 之间的串扰增强了 IgG 和补体片段调理的靶标的吞噬作用。这种协同作用首先在自身免疫性溶血性贫血模型中被注意到,其中补体激活增加了 IgG 调理子化红细胞 (RBC) 的清除率。研究表明,与 IgG 和 C3b 联合调理会导致更高的吞噬率和中性粒细胞产生的炎性细胞因子。
ADCP治疗人类恶性肿瘤
治疗性单克隆抗体可以通过各种机制诱导细胞毒性,包括 ADCP。利妥昔单抗是一种原型抗 CD20 单克隆抗体,通过诱导 ADCP 有效治疗 B 细胞恶性肿瘤。然而,其单药治疗效果有限,通常需要与化疗或其他靶向治疗联合使用。例如,将利妥昔单抗与化疗或布鲁顿酪氨酸激酶 (BTK) 抑制剂等靶向药物联合使用,可改善慢性淋巴细胞白血病 (CLL) 的临床结果。
来自小鼠模型的机理见解
小鼠模型为ADCP的机制提供了宝贵的见解。研究表明,肝脏和脾脏中固定的巨噬细胞在通过ADCP清除循环B细胞方面起着重要作用。抗 CD20 mAb 的疗效取决于 FcγRs 对巨噬细胞的激活。肝脏中的 Kupffer 细胞已被确定为抗 CD20 mAb 处理后从循环中清除 B 细胞的关键效应因子。
限制ADCP疗效的因素
有几个因素限制了ADCP在体内的功效:
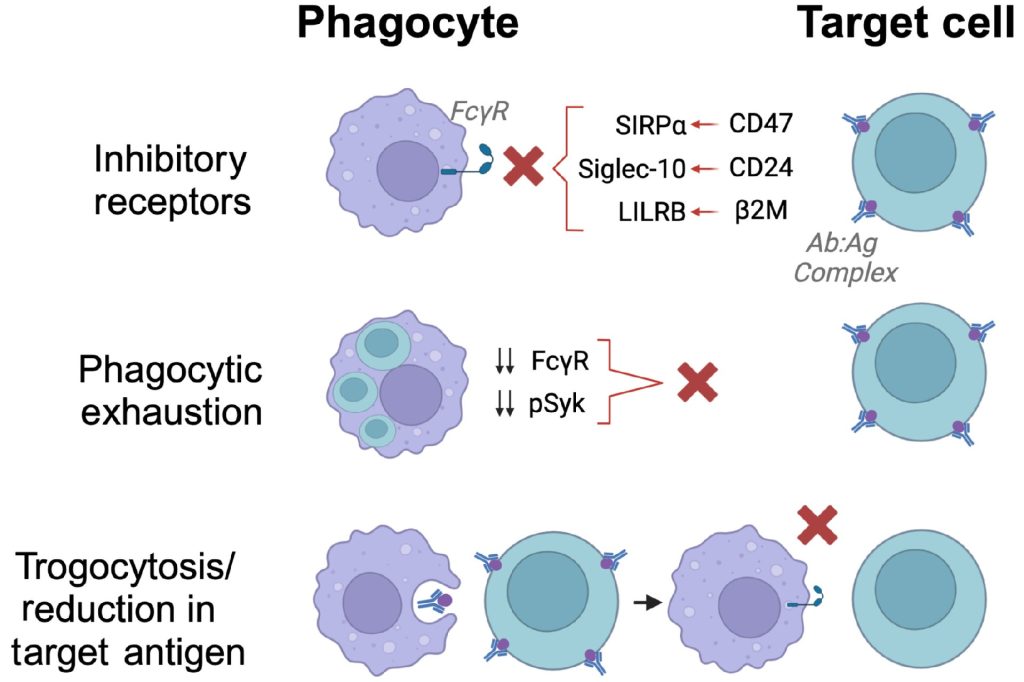
- 抑制性受体:FcγRIIb 是唯一的抑制性 FcγR,通过募集使关键信号分子去磷酸化的磷酸酶来抑制 FcγR 介导的吞噬作用。吞噬细胞上的激活信号和抑制信号之间的平衡决定了 ADCP 阈值。
- 补体的局限性:癌症患者经常表现出补体蛋白的缺乏,而治疗性单克隆抗体会导致补体消耗,从而降低其疗效。在接受利妥昔单抗治疗的CLL患者中观察到补体消耗,导致细胞毒性活性降低。
- CD47 作为负调节因子:癌细胞上的 CD47 与巨噬细胞上的 SIRPα 相互作用,发出“不要吃我”的信号,抑制吞噬作用。CD47 高表达与 mAb 疗效不佳有关。阻断 CD47-SIRPα 轴已显示出增强 mAb 诱导的各种癌症吞噬作用的前景。
- 吞噬能力耗尽:巨噬细胞在广泛的吞噬作用后会变得“疲惫”,失去吞噬其他靶标的能力。这种耗竭与巨噬细胞表面 FcγR 的下调有关。克服吞噬能力衰竭的策略可以提高mAb的治疗效果。
- 靶抗原丢失:恶性细胞可以下调或脱落靶抗原,从而降低它们对mAb诱导的细胞毒性的易感性。滋养细胞作用,其中免疫复合物从靶细胞中去除而不被吞噬,有助于这种抵抗机制。
- 药代动力学:mAb的大尺寸限制了它们对组织的渗透,影响了它们到达和清除靶细胞的能力。需要增强组织渗透策略来提高mAb的功效。
- 效应细胞与靶细胞的比率:效应细胞(例如巨噬细胞)与靶细胞的比率会影响 ADCP 的有效性。高肿瘤细胞载量会使可用的效应细胞不堪重负,从而降低 mAb 的功效。调节单个巨噬细胞的细胞毒性活性可以改善恶性细胞的清除率。
- ADCP的免疫调节:FcγR激活可以诱导促炎环境,但FcγR依赖性ADCP在调节巨噬细胞反应中的作用仍未得到充分研究。ADCP可导致抗炎细胞因子的释放,从而可能损害适应性免疫反应。从ADCP中解耦细胞因子释放可以提高mAb的治疗效果。
克服 ADCP 限制的策略
正在探索几种方法来提高ADCP的疗效:
- 抗体工程:Fc工程可以修饰mAb,以提高其对FcγR或补体激活的亲和力。Fc-脱岩糖基化增加FcR亲和力,增强吞噬作用。促进抗原连接单克隆抗体六聚化的 Fc 突变可以促进补体激活和吞噬作用。
- 靶向抑制通路:阻断CD47-SIRPα轴可以与mAb疗法协同作用,改善临床结果。几种抗 CD47 和抗 SIRPα 单克隆抗体目前正在进行临床试验,显示出在增强 ADCP 和整体 mAb 疗效方面的潜力。
- 新型治疗方案:将单克隆抗体与先天免疫检查点抑制剂(如抗 CD47 抗体)联合使用已显示出改善淋巴瘤的反应。优化单克隆抗体给药方案以避免对先天免疫细胞毒性和抗原损失的长时间抑制,可以提高治疗效果。
总之,ADCP代表了mAb诱导的癌症免疫治疗中细胞毒性的强大机制。了解限制ADCP疗效的因素并制定克服这些障碍的策略,将增强mAb在治疗恶性肿瘤方面的治疗潜力。
参考资料:
Van Wagoner, CM, Rivera-Escalera, F., Jaimes-Delgadillo, NC, Chu, CC, Zent, CS, & Elliott, MR (2023).癌症免疫疗法中抗体介导的吞噬作用。免疫学评论,319(1),128-141。https://doi.org/10.1111/imr.13265